II型聚酮合酶(PKSs)是一种独立的单功能酶,它们形成多酶复合物能够组装各种生物活性芳香天然产物,如临床重要的阿霉素、四环素和光神霉素等等。在典型II型PKS体系中,聚酮合酶(KS)和链长因子(CLF)形成异源二聚体(KS-CLF),反复催化多轮脱羧Claisen缩合反应,生成与酰基载体蛋白(ACP)连接的聚酮酰硫酯中间体。全长的聚酮中间体在酮基还原酶(KRs)、环化酶(CYCs)和芳香化酶等辅酶的作用下进行折叠,从而形成芳香化合物。而近年来出现了一类特殊的高度还原的II型聚酮合酶(HR Type II PKSs),其被证实参与了多烯类化合物的生物合成。例如对多烯化合物ishgamide的体外生化研究表明,一个HR Type II PKSs负责了其生物合成。Iga II型PKS系统的核心酶与典型II型PKS系统有很多共同之处,但有额外的KR和脱水酶(DH)。KR和DH可重复催化ACP上底物的β-酮基还原和脱水形成双键,最终经过多次延伸循环后形成多烯化合物。

此外,近几年有少量含肉桂酰基团的天然产物(CCNPs)被报道,例如skyllamycin, WS9326A, haoxinnamide, pepticinnamin, atratumycin, youssoufene等等均具有抗菌、细胞毒和抗结核活性。肉桂酰基团的生物合成被认为是由一种特殊的高度还原(HR)的II型聚酮合成酶(PKS)催化的(Scheme 1)。然而,其生物合成路线,特别是苯环形成的环化步骤仍不清楚。
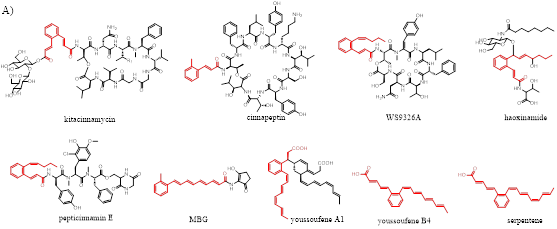
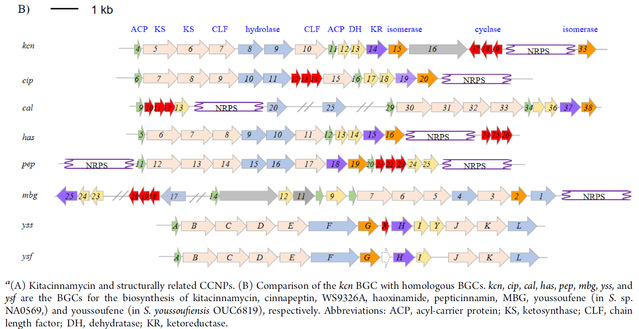
在前期的研究中,我们通过基因挖掘发现了一类含有肉桂酰基团的糖肽类化合物kitacinnamycins(Chem. Sci., 2019, 10, 4839-4846.)。鉴于这些CCNPs中特殊肉桂酰基团的生物合成步骤一直未被研究清楚,于是我们以kitacinnamycin为模型化合物尝试破译其生物合成路线。在本研究中,我们表达并获得了kcn基因簇上HR Type II PKS相关的蛋白,在体外成功重构了kitacinnamycin中肉桂酰基团的合成。简言之,ACP、KS/CLF、KR、DH以乙酰辅酶A和丙二酰辅酶A作为底物,经三轮延伸后合成了C8-三烯化合物;继而在异构酶的作用下第三个双键发生异构,随后又经历两轮延申形成C12-五烯底物;最后三蛋白复合体Kcn17−Kcn18−Kcn19可以催化C12-五烯底物发生6π-电环化并脱氢生成苯环(Figure 1)。
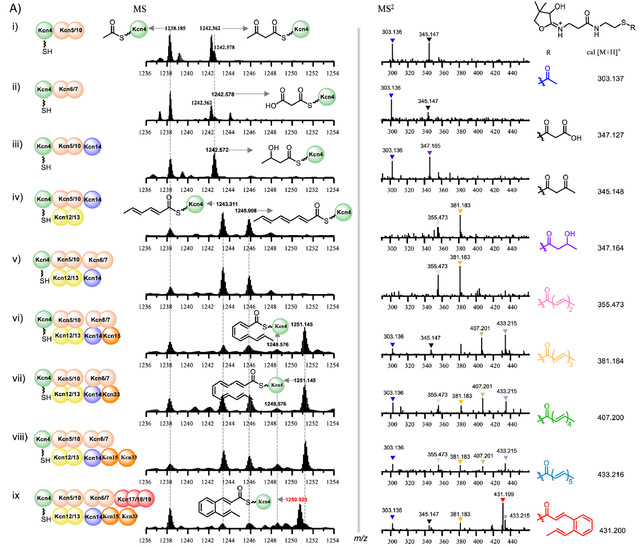
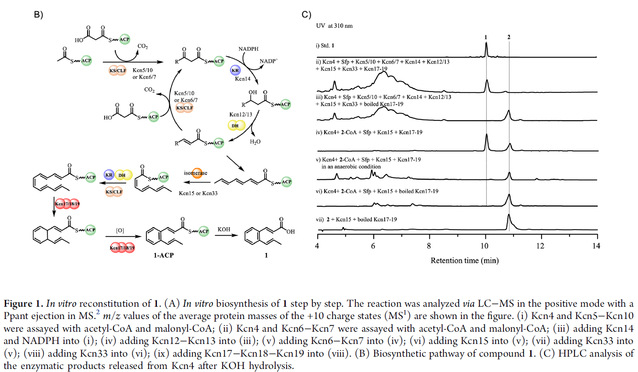
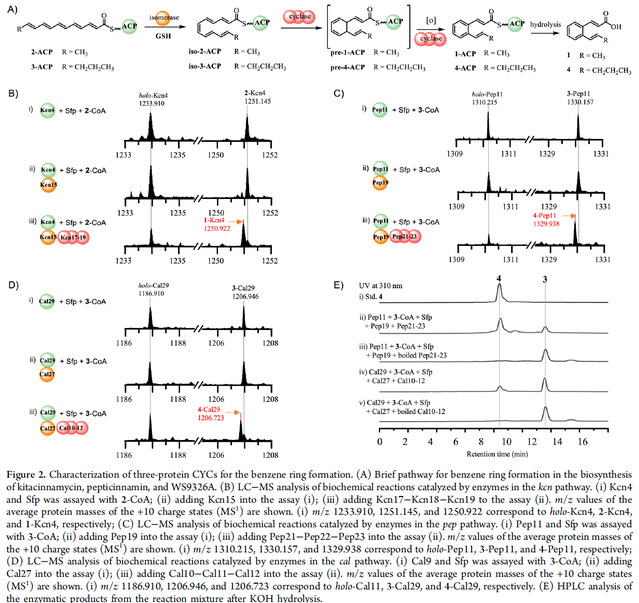
受到Kcn17-Kcn18-Kcn19催化功能的鼓舞,我们考虑是否其他同源蛋白也可以催化苯环的形成。于是表达了化合物pepticinnamin和WS9326A生物合成基因簇上的相关蛋白,且化学合成了可能的多烯底物2和3。将2和3连在相应ACP上作为底物,体外验证相应的异构酶和三蛋白复合体的功能,均能产生相应的环化产物。因此,我们的结果表明,三种蛋白复合物Pep21-Pep22-Pep23和Cal10-Cal11-Cal12,分别负责pepticinnamin和WS9326A生物合成中肉桂酰部分苯环的形成。(Figure 2)
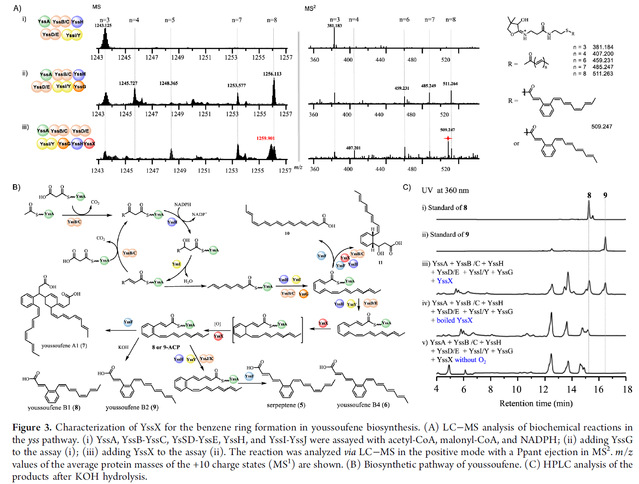
与这些通过酰胺键与氨基酸残基结合的肉桂酰部分不同,youssoufene是独特的游离肉桂酸类。先前有文献报道youssoufene生物合成过程中的多烯中间体由HR Type II PKS负责催化形成,然而负责苯环形成的酶仍是未知的。我们发现在其生物合成基因簇中并没有Kcn17-Kcn18-Kcn19的同源蛋白,但是与已报道的ysf基因簇相比,我们的yss基因簇上多了一个仅含有59个氨基酸的小蛋白YssX。敲除yssX后,终产物不再产生,证明YssX与youssoufene的生物合成相关。为验证YssX的功能,我们在体外重构了youssoufene的生物合成过程,与Kcn17-Kcn18-Kcn19功能类似,YssX催化了苯环的形成。至此我们阐明了youssoufene的完整生物合成路径。(Figure 3)
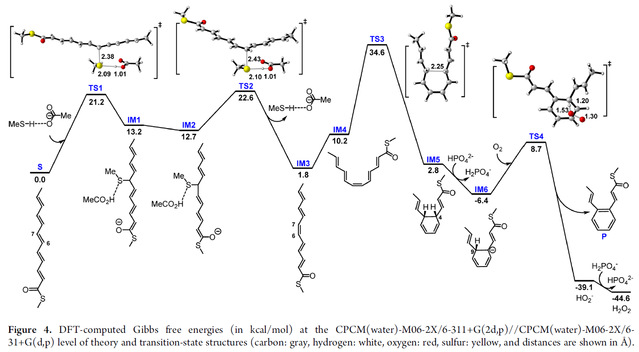
了更好地理解苯环形成的反应机理,我们对从多烯S(模拟2-ACP)开始的一系列反应进行了密度泛函理论(DFT)计算,进一步支持了三蛋白复合体Kcn17-19或蛋白YssX在生物合成中的催化作用。(Figure 4)
综上,在这项工作中,我们在体外重组了肉桂酰基团的生物合成,并将这些发现扩展到了其他的CCNPs,揭示了长期以来在肉桂酰生物合成中苯环形成的奥秘。尽管苯环在自然产物中几乎无处不在,但其生物合成并不容易,自然界采用了两种主要的方法合成苯环:(1)莽草酸途径是芳香族氨基/羟基酸生成的常见途径,这些芳香族氨基/羟基酸是大多数生物生成苯衍生物的主要来源;(2)另一种途径是通过PKSs催化活性聚酮骨架发生环化得到。
本研究首次证明了两个系统发育完全不同的环化酶可以通过多烯前体合成苯环。其中三蛋白复合体催化的环化代表了CCNPs中形成苯环的一种相对常见的策略,因为至少有6个已知的加上207个未鉴定的生物合成基因簇中都包含这种三基因操纵子,而YssX是一种单独的酶,只在youssoufene生物合成过程中负责苯环的形成。本研究的结果拓展了我们对芳香环生物合成的认识,为CCNPs的进一步基因组挖掘和组合生物合成奠定了基础。
伟德BETVlCTOR1946的副研究员史净博士为文章的第一作者,伟德BETVlCTOR1946的戈惠明教授、谭仁祥教授和BETVLCTOR伟德官网下载化学化工学院的梁勇教授为文章的通讯作者。该研究得到了国家重点研发计划、国家自然基金委杰出青年基金、国家自然基金委青年基金及中央高校基本科研业务费等项目的资助。
原文链接:https://pubs.acs.org/doi/pdf/10.1021/jacs.2c02855
文章题目:In Vitro Reconstitution of Cinnamoyl Moiety Reveals Two Distinct
Cyclases for Benzene Ring Formation