β-内酯类化合物是一类含四元内酯结构的分子,在自然界中鲜有报道,由于β-内酯环固有的高张力,使其很容易被蛋白上的亲核基团所进攻,从而导致开环,形成共价键,因此,β-内酯是一种理想的药效基团,可用于开发高效的酶抑制剂。例如,链霉菌所产生的β-内酯化合物lipstatin 的是胰腺脂肪酶的强效共价抑制剂,其四氢衍生物orlistat(奥利司他)已被FDA 批准用于治疗肥胖症。Salinosporamide A 是一种从海洋盐孢菌中分离出来的β-内酯化合物,是一种20S 蛋白酶体不可逆共价抑制剂,目前正处于治疗多发性骨髓瘤和其他晚期恶性肿瘤的III期临床试验中。因此,β-内酯化合物是一类极具吸引力的天然产物,不仅具有独特的结构特征,还具有潜在的生物活性。
近期,伟德BETVlCTOR1946戈惠明课题组在《自然-合成》(Nature Synthesis)发表了题为“Discovery and biosynthetic pathway analysis of cyclopentane–β-lactone globilactone A ”的研究论文。该研究从链霉菌中通过基因组挖掘发现了一类新型环戊烷-β-内酯化合物,并揭示了其独特的环戊烷-β-内酯双环结构的装配线上形成过程。
<推送封面图>
研究人员利用基因组挖掘方法在链霉菌Streptomyces globisporus NPDC060234 的基因组中发现了一条PKS/类NRPS杂合的基因簇glo,通过异源表达及发酵分离,从中鉴定了一个包含环戊烷-β-内酯化合物 globilactone A(1)及两个β-内酯开环衍生物globilactone B(2)和C(3)(图1)。活性实验结果显示化合物1对A类的β-内酰胺酶具有一定的抑制作用,IC50 值为15.05 μM。
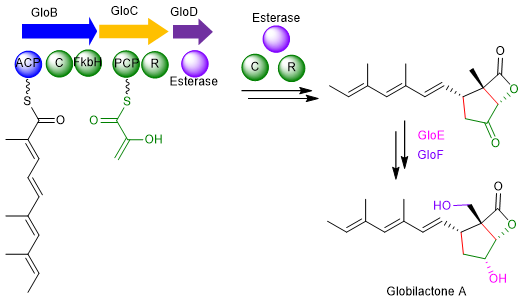
根据文献报道,仅有3例β-内酯类化合物的成环机制被研究清楚:obafluorin,vibralactone和salinosporamide A。Globilactone A中独特的双环结构促使研究人员对其生物合成过程展开了研究。通过基因敲除和代谢产物分析,研究人员对其生物合成过程进行了推测,主要包括两个方面,一个是装配线上的骨架形成过程,另一个是线下的后修饰过程。根据突变菌株中的代谢产物分离及体外酶反应实验表明,线下的后修饰过程包括C15位羰基的还原,由短链脱氢酶GloE催化;以及C12位的羟基化,由P450蛋白GloF负责。当C15位羰基未被还原时,β-内酯环容易被N-乙酰基-半胱氨酸进攻开环,形成对应的化合物2和3(图1)。

图1 globilactone A-C(1-3)生物合成过程推测
首先,作者对线上的骨架形成过程进行了研究,其骨架包括两部分:一部分是由聚酮合成酶合成的聚酮链,另一部分是甘油酸酰基来源的三碳单元。研究人员通过投喂全碳标记的葡萄糖([13C6]-glucose)进行了验证,证实该三碳单元来源于糖酵解途径的1,3-二磷酸甘油酸,经FkbH识别并转移至PCP进入装配线。关于两部分是如何构建的双环骨架,作者提出了两条路线,通过投喂C1标记的葡萄糖([1-13C]-glucose)及产物分离鉴定,表明其成环过程是经路线ii进行的(图2)。

图2 a.环戊烷-β-内酯两种成环路线推测;b.投喂标记葡萄糖及对应分离产物。
为了进一步研究其双环结构的成环机制,研究人员表达了相关蛋白,并合成了对应的线性聚酮链作为底物进行酶反应,成功在体外重构了化合物3的生成(图3a)。同时,研究人员将合成的标记的甘油酸作为1,3二磷酸甘油酸的前体进行了酶反应,得到了对应的标记产物3c和中间体12’,进一步证实了该反应中间体(图3d)。
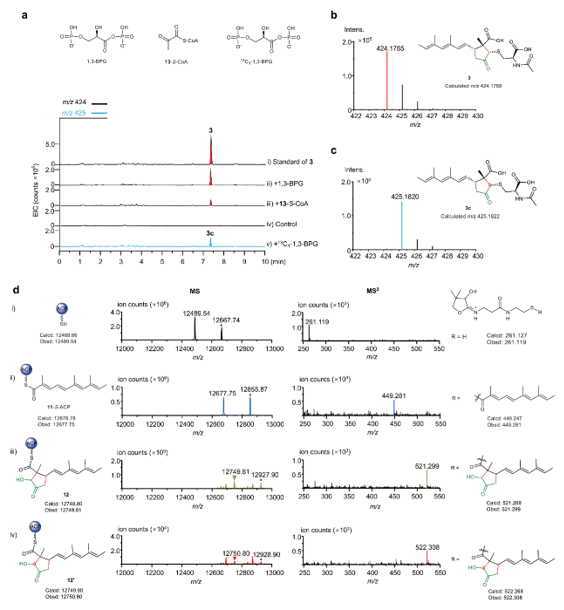
图3 体外重构globilactone B(3)及LC-MS分析酶反应产物
随后,研究人员通过化学衍生化实验和蛋白点突变实验揭示了双环结构的形成过程,首先是FkbH domain的作用下对三碳单元进行脱水,然后由C domain催化迈可尔加成,形成了第一个碳-碳键C10-C16,然后R domain将PCP domain上的硫酯还原成醛基,引发了aldol加成,形成了第二个碳-碳键C11-C14,然后反应中间体转移到酯酶上,由酯酶催化酯化反应形成β-内酯并从蛋白上解离下来生成中间体6,随后进入后修饰过程。
最后,作者以GloC和GloD为探针进行了基因组挖掘,共找到7株含有glo同源基因簇的菌株,通过异源表达,作者发现其中两株菌可以产生这类化合物,并分离得到了一个新的β-内酯开环产物。
该工作通过体内体外实验揭示了其PKS和类NRPS 装配线形成环戊烷-β-内酯的生化机制,表明类NRPS 模块具有显著的功能多样性,丰富了β-内酯的形成策略,为指导未来的基因组挖掘和基于 β-内酯的天然产物的化学酶法合成提供了基础。
伟德BETVlCTOR1946博士后徐梓斐为文章第一作者,伟德BETVlCTOR1946戈惠明和谭仁祥教授为通讯作者。该研究得到了国家重点研发计划、国家自然基金及中央高校基本科研业务费等项目的资助。
原文链接:https://www.nature.com/articles/s44160-023-00414-3
文章题目:Discovery and biosynthetic pathway analysis of cyclopentane–β-lactone globilactone A